常州江苏大学工程技术研究院
Changzhou Engineering and Technology Institute of Jiangsu University
研究内容简介
通过生物材料推动骨感染的修复是科研工作者和临床医生面临的一大挑战。该研究利用糖肽类抗生素万古霉素(Van)及其靶向二肽D-Ala-D-Ala(AA)的天然可逆识别策略,设计了开发了一种模拟骨折周围血肿的含成骨生长肽(OGP)动态网络水凝胶系统,用于感染性骨折修复。结果显示:该仿血肿水凝胶系统具有有效杀菌和促成骨分化的能力。进一步研究表明,该水凝胶系统可实现局部炎症微环境重塑,同步抑制感染、促骨形成,实现自然和功能性骨愈合。(图1)
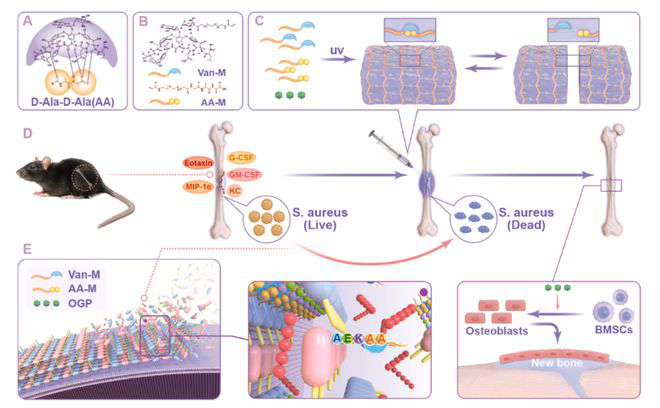
图1. Van-AA-OGP水凝胶的合成和应用以及杀菌和成骨作用机理的示意图。
研究者通过NHS-酯交联反应,制备了Van单体与AA单体,进而经光引发聚合反应合成Van-AA-OGP水凝胶体系。形态学实验验证了该水凝胶的可注射性、自愈合性(Fig. 2D, E, I)。流变学显示,Van-AA-OGP水凝胶的粘弹性与血肿相似(Fig. 2J-K)。此外,Van-AA-OGP水凝胶体系还显示出显著的杀菌效果(Fig. 2N),且保留了良好的生物学活性(Fig. 2P)

图 2.Van-AA-OGP水凝胶的动态性,杀菌性能和生物相容性。
体外研究显示,Van-AA-OGP水凝胶体系促进了系列成骨相关基因和蛋白的表达(Fig. 3B-G, J),且在诱导分化7天及14天后分别促进了碱性磷酸酶的表达和钙结节的形成(Fig. 3A, H, I),促进了成骨分化进程。
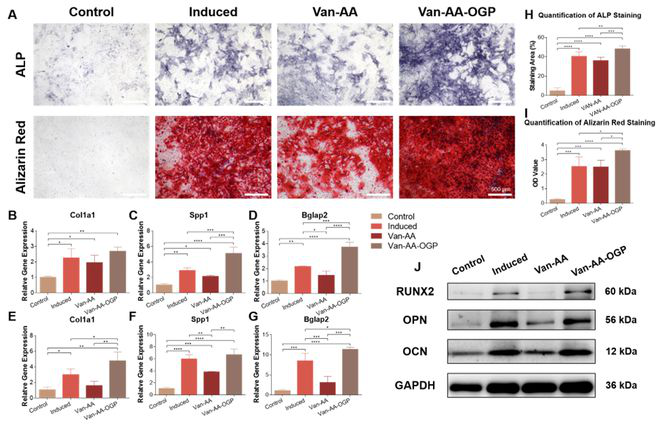
图 3.Van-AA-OGP水凝胶在体外促进成骨分化。
为了探究Van-AA-OGP水凝胶体系在体内的抗菌效果,研究者建立了小鼠股骨感染性骨折模型,针对感染性骨折局部组织进行了进一步评估,吉姆萨染色、革兰染色、免疫荧光染色以及组织提取物的菌落分析均证实,Van-AA-OGP水凝胶体系在体内保持了良好的抗菌性能,有效清除组织致病菌(图4)。
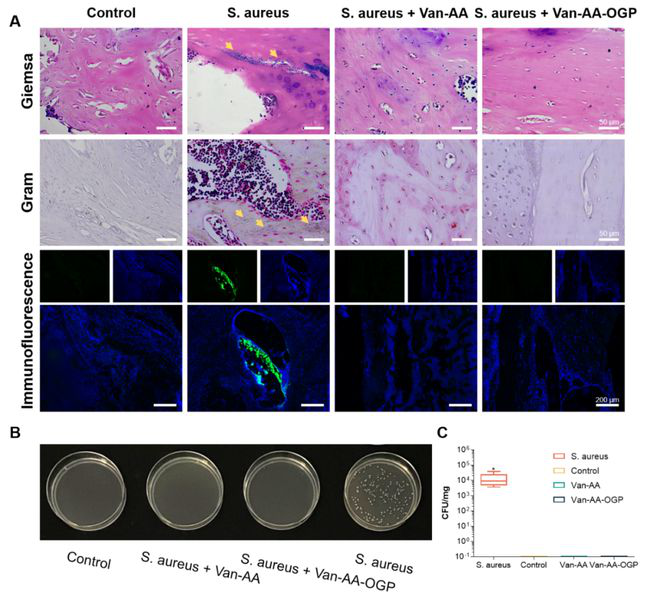
图 4.Van-AA-OGP水凝胶在体内的杀菌性能。
进一步对体内局部炎症微环境进行研究发现,金葡菌感染的炎症微环境存在大量促炎细胞因子和巨噬细胞、T细胞募集,表现出局部微环境中异常的长期炎症反应和典型的适应性免疫进程。Van-AA-OGP水凝胶体系在体内扭转了感染进程中的炎症微环境,重塑正常局部微环境,从而有效恢复了生理性骨愈合进程(图5)。
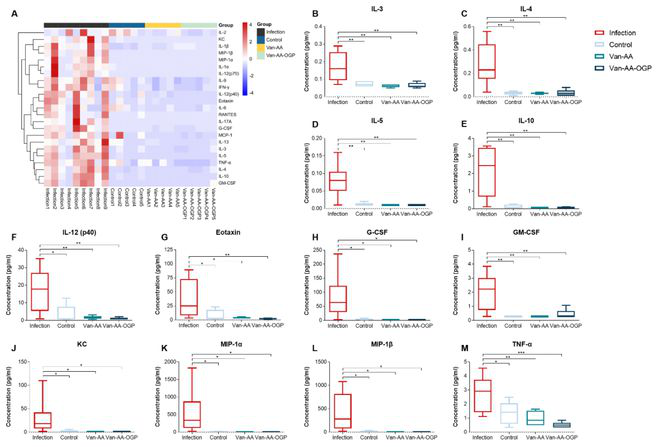
图 5.感染性骨折4周后体内炎症微环境分析。
在小鼠感染性骨折模型中,Van-AA-OGP水凝胶体系有效发挥促骨形成的功能,促进长骨骨折的生理性愈合,加速软骨内成骨的骨成熟进程,重塑长骨的完整结构并提升骨骼强度(图6、7)。
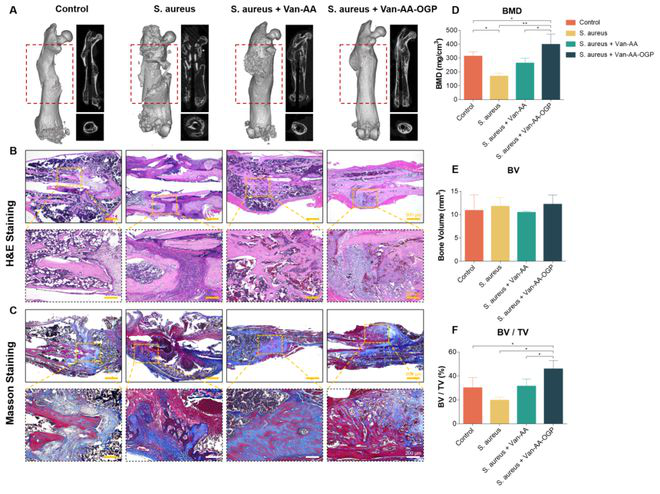
图 6.感染性骨折4周后组织学及影像学评价
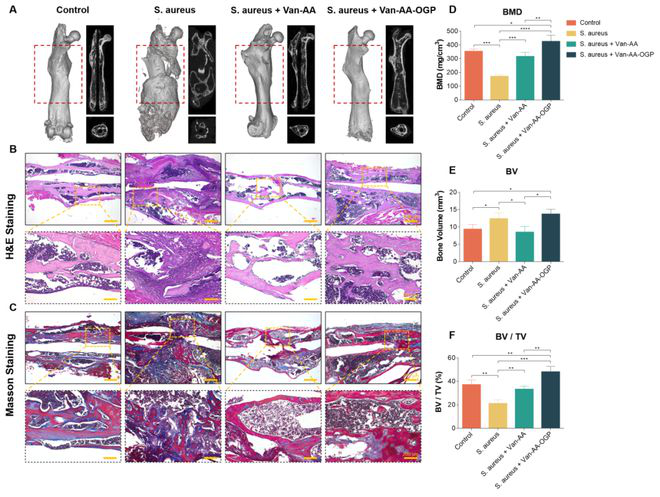
图 7.感染性骨折8周后组织学及影像学评价
综上所述,本研究使用分子识别策略开发了一种模拟血肿的动态水凝胶网络。清除局部致病菌,恢复炎症微环境,促进骨折愈合。为治疗感染性的骨折杀菌生物材料提供新的思路。